Wie funktioniert Strom? Warum leiten manche Materialien und andere nicht und warum halten Atome zusammen? Wenn du dich mit diesen Fragen befasst, dann sprecht ihr im Unterricht wahrscheinlich gerade über das Thema Elektronen. Für dich klingt das alles noch ziemlich abstrakt?
Kein Problem, in unserem Artikel zeigen wir dir:
- …was Elektronen sind.
- …welche Eigenschaften sie haben.
- …warum diese Elementarteilchen für unser modernes Leben unverzichtbar sind.
- Es ist unbekannt ob Elektronen aus anderen Komponenten bestehen, deshalb werden sie auch als Elementarteilchen bezeichnet.
- Sie sind negativ geladen und ihre Ladung wird auch Elementarladung genannt.
- Die negativen Teilchen gehören zur Leptonengruppe.
- Elektronen werden auch als subatomare Teilchen bezeichnet, da sie gemeinsam mit Protonen und Neutronen ein Atom bilden.
- Sie müssen aber nicht an ein Atom gebunden sein, sondern können auch frei auftreten.
- Ein Elektron hat einen Wellen– und einen Teilchencharakter (wie alle anderen Elementarteilchen auch): Dadurch können sie mit anderen Teilchen kollidieren, aber auch gebeugt werden wie Licht.
Diese negativ geladenen Teilchen spielen in verschiedenen Aspekten der Physik, Chemie und Technologie eine entscheidende Rolle.
Die Elementarteilchen sind verantwortlich für Elektrizität und elektrischen Strom außerdem bestimmen sie die Eigenschaften von Materialien (z.B. Leitfähigkeit).
Die Elektronen sind entscheidend für die Bildung von Molekülen und chemischer Bindungen zwischen Atomen.
Sie sind an Strahlungsprozessen (Emission = Abgabe und Absorption = Aufnahme von Licht) beteiligt.
Welche Funktion haben die negativen Elementarteilchen in einem Atom?
- Zusammensetzen der Elektronenhülle: die Elektronen, die durch die Coulomb Kraft an ein Atom gebunden sind, bilden die Hülle.
- Bildung von Molekülen und chemischen Verbindungen: dies geschieht durch die gemeinsame Nutzung bzw. das Übertragen der negativen Teilchen zwischen Atomen.
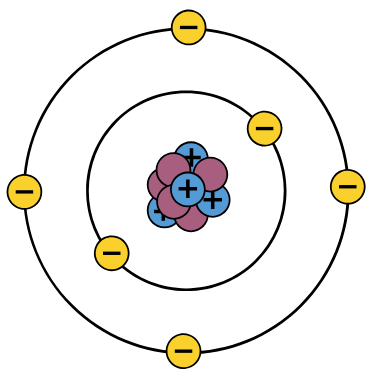
⇒ Die Basis chemischer Bindungen sind elektromagnetische Wechselwirkungen.
Wie bewegen sich Elektronen um den Atomkern?

Elektronen bewegen sich nicht auf festen Bahnen, sondern sie befinden sich in sogenannten Orbitalen.
- Je nach Größe und Energie des Elektrons haben die Orbitale eine unterschiedliche Form.
Angezogen werden die Elektronen von dem positiv geladenen Atomkern.
Elektronen Eigenschaften – eine kompakte Übersicht

Masse der negativ geladenen Elementarteilchen
Elektronen weisen die kleinste Masse der ladungstragenden Leptonen auf und machen lediglich 0,1% der Gesamtmasse eines Atoms aus.
Masse eines einzelnen Elektrons:![]()
⇒ entspricht circa: ![]()
u ist die Einheit für die atomare Masseneinheit.
Ladung der Elektronen
Ein Elektron besitzt die kleinste in der Natur vorkommende Ladung. Dennoch ist diese fundamental in der Physik.
Sie hat einen Wert von: ![]()
Bezeichnet wird sie auch als e- für Elementarladung: ![]()
Durch die Ladung, die diese Elementarteilchen tragen, entsteht ein elektrisches Feld. Wird ein Elektron dann in Bewegung versetzt, entwickelt sich ein magnetisches Feld. Wenn nun ein Elektron in ein anderes elektrisches Feld gelangt, beeinflusst die Lorentzkraft seine Bahn.
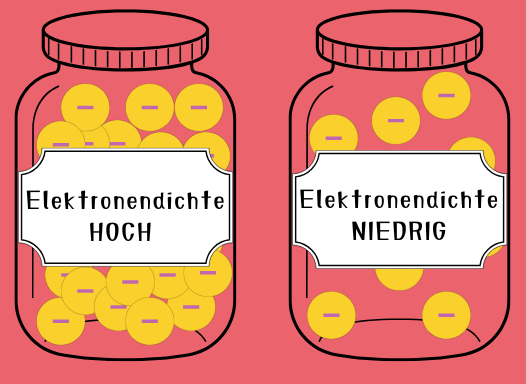
Elektronendichte
Je höher die Elektronendichte ist, desto mehr negative Teilchen sind in einem bestimmten Volumen vorhanden.
Intrinsisches Drehmoment der Elektronen
- Das intrinsische Drehmoment beeinflusst das Verhalten des Elektrons in magnetischen und elektrischen Feldern.
- Der Spin führt dazu, dass das Elementarteilchen wie ein winziger Magnet wirkt.
→ Elektronen besitzen einen Spin von 1/2, wie alle Leptonen. Sie sind dadurch der Gruppe der Fermionen zuzuordnen und unterliegen dem Pauli-Prinzip.
→ Dieses Prinzip besagt, dass zwei Elektronen nur dann denselben Energiezustand einnehmen, wenn ihre Spins gegensätzlich sind.

Die winzigen Ladungsträger und ihre Energie
Die Ruheenergie eines Elektrons beträgt 0,511 MeV (Mega-Elektronen-Volt).
Wie du bereits weißt bilden Elektronen, die an ein Atom gebunden sind, eine Elektronenhülle. Die Elektronen befinden sich dabei in Kugelschalen. Diese Schalen stellen verschiedene Energieniveaus dar.
Leitfähigkeit der Elektronen
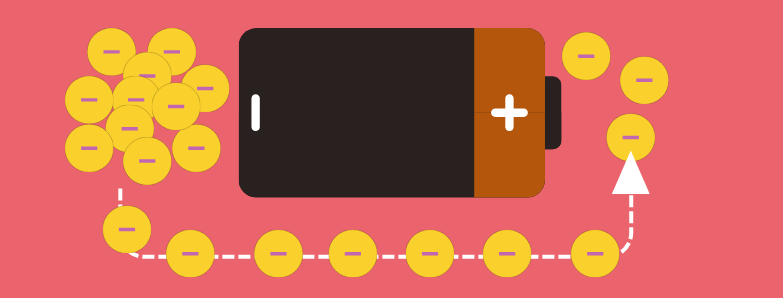
Einfach ausgedrückt hängt die Leitfähigkeit eines Materials davon ab, wie frei sich Elektronen darin bewegen können.
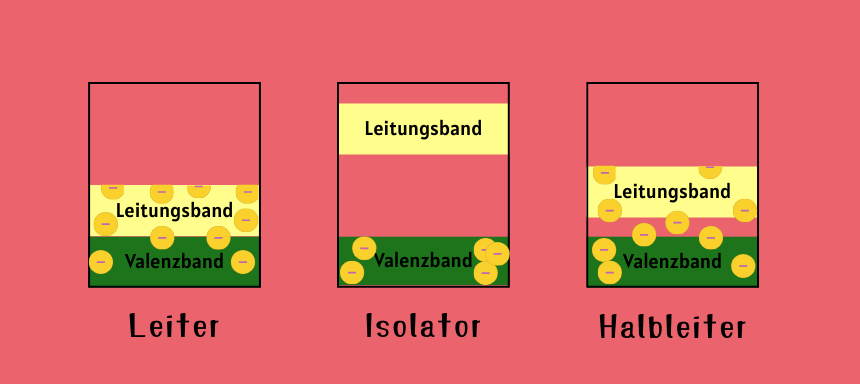
Ein Stromfluss in elektrischen Leitern wird folgendermaßen erzeugt:
- Im Leiter herrscht ein Ungleichgewicht:
- Minuspol: Elektronenüberschuss
- Pluspol: Elektronenmangel
- Der Potentialunterschied verursacht ein elektrisches Feld, das dazu führt, dass die Elektronen in Bewegung gesetzt werden.
- Elektronen bewegen sich einzeln von einem Atom zum anderen.
- Dabei zirkulieren sie vom Minuspol zum Pluspol des Leiters.
Der Unterschied zwischen den Ladungen am Minus- und Pluspol wird auch als Spannung definiert (angegeben wird sie in Volt). Diese gibt an, wie viel Energie zugeführt werden muss, damit sich die Elektronen bewegen.
In einem Isolator sind die negativen Teilchen fest an ihre Atome gebunden und können sich nicht frei bewegen.
Im Falle eines Halbleiters ist die Beweglichkeit der Elektronen z.B. durch Temperaturveränderungen und elektrische Spannung zu beeinflussen. Deshalb können Halbleiter einerseits als Leiter dienen, andererseits aber auch Isolatoren sein.
Damit dieser Wechsel möglich ist, befindet sich in Halbleitern eine Energiebandlücke zwischen dem Valenzband (darin sind die Elektronen gebunden) und dem Leitungsband (Elektronen können sich frei bewegen).
⇒ Die Bandlücke gibt an, wie viel Energie erforderlich ist, damit Elektronen Strom leiten können.
Warum sind Elektronen wichtig für elektrische Ströme?
Elektronen sind Ladungsträger, die sich in einem Leiter bewegen. Dadurch wird ein Stromfluss erzeugt. Somit sind sie grundlegend für elektrische Ströme.
Die Stärke des Stroms (wird in Ampere gemessen) ist abhängig von der Anzahl der negativen Ladungsträger, die durch den Leiter fließen.
Elektronen im Periodensystem
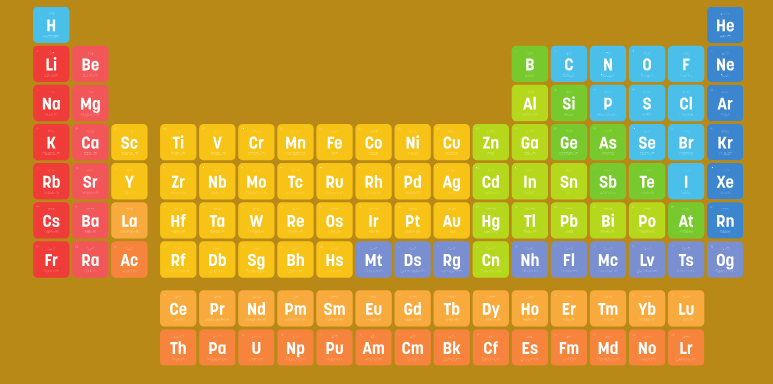
Die Verteilung der Elektronen in der Elektronenhülle…
• …bestimmt die Position des Elements im Periodensystem.
• …ist entscheidend für die chemischen Eigenschaften und das Bindungsverhalten des Elements
Diese gibt bei neutralen Atomen die Anzahl der Protonen als auch die der Elektronen an.
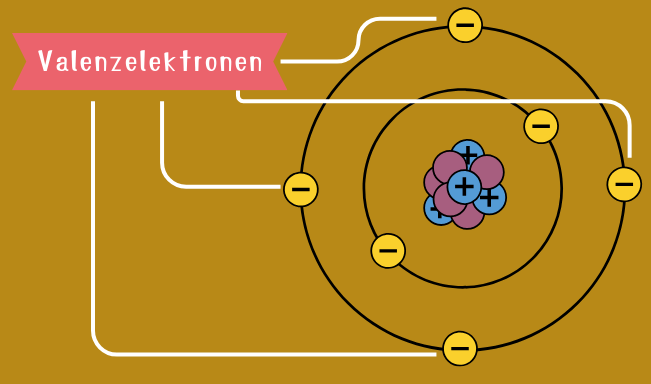
Elektronen ordnen sich in Schalen und Orbitalen (z.B. s-, p-, d-, f- Orbitale) um den Atomkern herum an. Jede Schale kann dabei eine bestimmte Anzahl an negativen Teilchen aufnehmen.
Sind die Elektronen, die sich in der äußersten Schale eines Atoms befinden.
Sie sind ausschlaggebend für das chemische Verhalten und die Bindungsfähigkeit eines Elements.
Bei Hauptgruppenelementen ist die Anzahl der Valenzelektronen identisch mit der Gruppennummer.
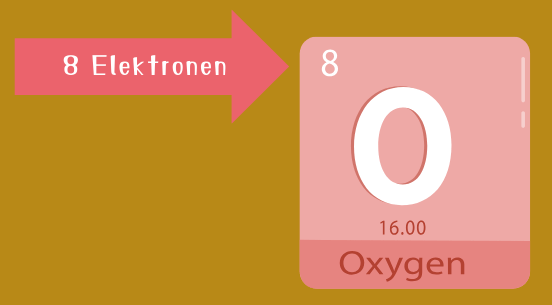
Diese gibt die genaue Verteilung der Elektronen auf Schalen und Orbitale an. Z.B. Sauerstoff: ![]()
Elektronen, Protonen, Neutronen



